- Внутрішня енергія тіл Згідно MKT всі речовини складаються з частинок, які знаходяться в безперервному...
- Зміна внутрішньої енергії
- механічна робота
- ізобарний процес
- Чи не ізобарний процес
- кількість теплоти
- Нагрівання (охолодження)
- Випаровування (конденсація)
- Плавлення (кристалізація)
- згоряння палива
- література
Внутрішня енергія тіл
Згідно MKT всі речовини складаються з частинок, які знаходяться в безперервному тепловому русі і взаємодіють один з одним. Тому, навіть якщо тіло нерухомо і має нульову потенційну енергію, воно має енергію (внутрішньою енергією), що представляє собою сумарну енергію руху і взаємодії мікрочастинок, що складають тіло. До складу внутрішньої енергії входять:
- кінетична енергія поступального, обертального і коливального руху молекул;
- потенційна енергія взаємодії атомів і молекул;
- внутрішньоатомна і внутрішньоядерна енергії.
У термодинаміки розглядаються процеси при температурах, при яких не порушується коливальний рух атомів в молекулах, тобто при температурах, які перевищують 1000 К. У цих процесах змінюються лише перші дві складові внутрішньої енергії. Тому
під внутрішньою енергією в термодинаміки розуміють суму кінетичної енергії всіх молекул і атомів тіла і потенційної енергії їх взаємодії.
Внутрішня енергія тіла визначає його тепловий стан і змінюється при переході з одного стану в інший. В даному стані тіло має цілком певною внутрішньою енергією, що не залежить від того, в результаті якого процесу воно перейшло в даний стан. Тому внутрішню енергію дуже часто називають функцією стану тіла.
Розрахувати внутрішню енергію можна тільки для ідеального газу, тому що молекули не взаємодіють між собою і потенційна енергія їх дорівнює нулю:
\ (~ U = \ dfrac {i} {2} \ cdot \ dfrac {m} {M} \ cdot R \ cdot T, \)
де i - ступінь свободи. Для одноатомного газу (наприклад, інертні гази) i = 3, для двоатомних - i = 5.
З цих формул видно, що внутрішня енергія ідеального газу залежить тільки від температури і числа молекул і не залежить ні від обсягу, ні від тиску. Тому зміна внутрішньої енергії ідеального газу визначається тільки зміною його температури і не залежить від характеру процесу, в якому газ переходить з одного стану в інший:
\ (~ \ Delta U = U_2 - U_1 = \ dfrac {i} {2} \ cdot \ dfrac {m} {M} \ cdot R \ cdot \ Delta T, \)
де Δ T = T 2 - T 1.
- Молекули реальних газів взаємодіють між собою і тому мають потенційну енергією W p, яка залежить від відстані між молекулами і, отже, від займаного газом об'єму. Таким чином, внутрішня енергія реального газу залежить від його температури, обсягу і структури молекул.
* Висновок формули
Середня кінетична енергія молекули \ (~ \ left \ langle W_k \ right \ rangle = \ dfrac {i} {2} \ cdot k \ cdot T \).
Число молекул в газі \ (~ N = \ dfrac {m} {M} \ cdot N_A \).
Отже, внутрішня енергія ідеального газу
\ (~ U = N \ cdot \ left \ langle W_k \ right \ rangle = \ dfrac {m} {M} \ cdot N_A \ cdot \ dfrac {i} {2} \ cdot k \ cdot T. \)
З огляду на, що k⋅N A = R - універсальна газова стала, маємо
\ (~ U = \ dfrac {i} {2} \ cdot \ dfrac {m} {M} \ cdot R \ cdot T \) - внутрішня енергія ідеального газу.
Зміна внутрішньої енергії
Для вирішення практичних питань істотну роль грає не сама внутрішня енергія, а її зміна Δ U = U 2 - U 1. Зміна ж внутрішньої енергії розраховують, виходячи із законів збереження енергії.
Внутрішня енергія тіла може змінюватися двома способами:
- При здійсненні механічної роботи. а) Якщо зовнішня сила викликає деформацію тіла, то при цьому змінюються відстані між частинками, з яких воно складається, а отже, змінюється потенційна енергія взаємодії частинок. При непружних деформацій, крім того, змінюється температура тіла, тобто змінюється кінетична енергія теплового руху частинок. Але при деформації тіла відбувається робота, яка і є мірою зміни внутрішньої енергії тіла. б) Внутрішня енергія тіла змінюється також при його неупругом зіткненні з іншим тілом. Як ми бачили раніше, при неупругом зіткненні тіл їх кінетична енергія зменшується, вона перетворюється у внутрішню (наприклад, якщо вдарити кілька разів молотком по дроті, що лежить на ковадлі, - дріт нагріється). Мірою зміни кінетичної енергії тіла є, відповідно до теореми про кінетичної енергії, робота діючих сил. Ця робота може служити і заходом зміни внутрішньої енергії. в) Зміна внутрішньої енергії тіла відбувається під дією сили тертя, оскільки, як відомо з досвіду, тертя завжди супроводжується зміною температури тіл, що труться. Робота сили тертя може служити мірою зміни внутрішньої енергії.
- За допомогою теплообміну. Наприклад, якщо тіло помістити в полум'я пальника, його температура зміниться, отже, зміниться і його внутрішня енергія. Однак ніяка робота тут не відбувалася, бо не відбувалося видимого переміщення ні самого тіла, ні його частин.
Зміна внутрішньої енергії системи без здійснення роботи називається теплообміном (теплопередачей).
Існує три види теплообміну: теплопровідність, конвекція і випромінювання.
а) Теплопровідністю називається процес теплообміну між тілами (або частинами тіла) при їх безпосередньому контакті, обумовлений тепловим хаотичним рухом частинок тіла. Амплітуда коливань молекул твердого тіла тим більше, чим вище його температура. Теплопровідність газів обумовлена обміном енергією між молекулами газу при їх зіткненнях. У разі рідин працюють обидва механізму. Теплопровідність речовини максимальна в твердому і мінімальна в газоподібному стані.
б) Конвекція є теплопередачу нагрітими потоками рідини або газу від одних ділянок займаного ними об'єму в інші.
в) Теплообмін при випромінюванні здійснюється на відстані за допомогою електромагнітних хвиль.
Розглянемо більш докладно способи зміни внутрішньої енергії.
механічна робота
При розгляді термодинамічних процесів механічне переміщення макротел в цілому не розглядається. Поняття роботи тут пов'язується зі зміною обсягу тіла, тобто переміщенням частин макротела один щодо одного. Процес цей призводить до зміни відстані між частинками, а також часто до зміни швидкостей їх руху, отже, до зміни внутрішньої енергії тіла.
ізобарний процес
Розглянемо спочатку ізобарний процес. Нехай в циліндрі з рухомим поршнем знаходиться газ при температурі T 1 (рис. 1).
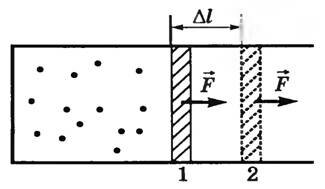
Мал. 1
Будемо повільно нагрівати газ до температури T 2. Газ буде ізобаріческі розширюватися, і поршень переміститься з положення 1 в положення 2 на відстань Δ l. Сила тиску газу при цьому зробить роботу над зовнішніми тілами. Так як p = const, то і сила тиску F = p⋅S теж постійна. Тому роботу цієї сили можна розрахувати за формулою
\ (~ A = F \ cdot \ Delta l = p \ cdot S \ cdot \ Delta l = p \ cdot \ Delta V, \)
де Δ V - зміна обсягу газу.
- Якщо обсяг газу не змінюється (Ізохоричний процес), то робота газу дорівнює нулю.
- Газ виконує роботу тільки в процесі зміни свого об'єму.
При розширенні (Δ V> 0) газу відбувається позитивна робота (А> 0); при стисненні (Δ V <0) газу відбувається негативна робота (А <0).
- Якщо розглядати роботу зовнішніх сил A '(А' = - А), то при розширенні (Δ V> 0) газу А '<0); при стисненні (Δ V <0) А '> 0.
Запишемо рівняння Клапейрона-Менделєєва для двох станів газу:
\ (~ P \ cdot V_1 = \ nu \ cdot R \ cdot T_1, \; \; p \ cdot V_2 = \ nu \ cdot R \ cdot T_2, \) \ (~ p \ cdot (V_2 - V_1) = \ nu \ cdot R \ cdot (T_2 - T_1). \)
Отже, при изобарном процесі
\ (~ A = \ nu \ cdot R \ cdot \ Delta T. \)
Якщо ν = 1 моль, то при Δ Τ = 1 До отримаємо, що R чисельно дорівнює A.
Звідси випливає фізичний зміст універсальної газової постійної: вона чисельно дорівнює роботі, яку здійснюють 1 моль ідеального газу при його изобарном нагріванні на 1 К.
Чи не ізобарний процес
На графіку p (V) при изобарном процесі робота дорівнює площі заштрихованого на малюнку 2, а прямокутника.
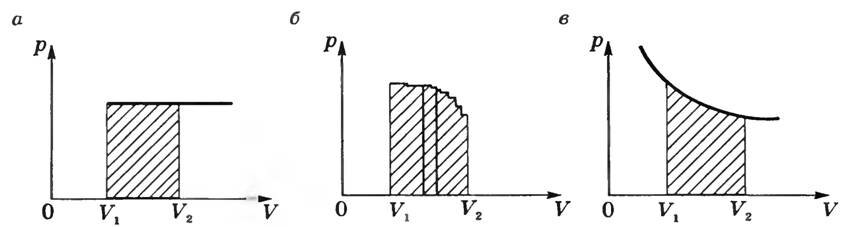
Мал. 2
Якщо процес не ізобарний (рис. 2, б), то криву функції p = f (V) можна уявити як ламану, що складається з великої кількості изохор і ізобар. Робота на ізохорно ділянках дорівнює нулю, а сумарна робота на всіх ізобарних ділянках буде дорівнює
\ (~ A = \ lim _ {\ Delta V \ to 0} \ sum ^ n_ {i = 1} p_i \ cdot \ Delta V_i \), або \ (~ A = \ int p (V) \ cdot dV, \ )
тобто буде дорівнює площі заштрихованої фігури.
При ізотермічному процесі (Т = const) робота дорівнює площі заштрихованої фігури, зображеної на малюнку 2, ст.
Визначити роботу, використовуючи останню формулу, можна тільки в тому випадку, якщо відомо, як змінюється тиск газу при зміні його об'єму, тобто відомий вид функції p = f (V).
Таким чином, видно, що навіть при одному і тому ж зміні обсягу газу робота буде залежати від способу переходу (тобто від процесу: ізотермічний, ізобарний ...) з початкового стану газу в кінцеве. Отже, можна зробити висновок, що
- Робота в термодинаміці є функцією процесу і не є функцією стану.
кількість теплоти
Як відомо, при різних механічних процесах відбувається зміна механічної енергії W. Мірою зміни механічної енергії є робота сил, прикладених до системи:
\ (~ \ Delta W = A. \)
При теплообміні відбувається зміна внутрішньої енергії тіла. Мірою зміни внутрішньої енергії при теплообміні є кількість теплоти.
Кількість теплоти - це міра зміни внутрішньої енергії в процесі теплообміну.
Таким чином, і робота, і кількість теплоти характеризують зміна енергії, але не тотожні внутрішньої енергії. Вони не характеризують сам стан системи (як це робить внутрішня енергія), а визначають процес переходу енергії з одного виду в інший (від одного тіла до іншого) при зміні стану і суттєво залежать від характеру процесу.
Основна відмінність між роботою і кількістю теплоти полягає в тому, що
- робота характеризує процес зміни внутрішньої енергії системи, що супроводжується перетворенням енергії з одного виду в інший (з механічною у внутрішню);
- кількість теплоти характеризує процес передачі внутрішньої енергії від одних тіл до інших (від більш нагрітих до менш нагрітих), що не супроводжується перетвореннями енергії.
Нагрівання (охолодження)
Досвід показує, що кількість теплоти, необхідне для нагрівання тіла масою m від температури T 1 до температури T 2, розраховується за формулою
\ (~ Q = c \ cdot m \ cdot (T_2 - T_1) = c \ cdot m \ cdot \ Delta T, \)
де c - питома теплоємність речовини (таблична величина);
\ (~ C = \ dfrac {Q} {m \ cdot \ Delta T}. \)
Одиницею питомої теплоємності в СІ є джоуль на кілограм-Кельвін (Дж / (кг · К)).
Питома теплоємність c чисельно дорівнює кількості теплоти, яку необхідно повідомити тілу масою 1 кг, щоб нагріти його на 1 К.
Крім питомої теплоємності розглядають і таку величину, як теплоємність тіла.
Теплоємність тіла C чисельно дорівнює кількості теплоти, необхідного для зміни температури тіла на 1 К:
\ (~ C = \ dfrac {Q} {\ Delta T} = c \ cdot m. \)
Одиницею теплоємності тіла в СІ є джоуль на Кельвін (Дж / К).
Випаровування (конденсація)
Для перетворення рідини в пару при незмінній температурі необхідно затратити кількість теплоти
\ (~ Q = L \ cdot m, \)
де L - питома теплота пароутворення (таблична величина). При конденсації пари виділяється така ж кількість теплоти.
Одиницею питомої теплоти пароутворення в СІ є джоуль на кілограм (Дж / кг).
Плавлення (кристалізація)
Для того щоб розплавити кристалічне тіло масою m при температурі плавлення, необхідно тілу повідомити кількість теплоти
\ (~ Q = \ lambda \ cdot m, \)
де λ - питома теплота плавлення (таблична величина). При кристалізації тіла така ж кількість теплоти виділяється.
Одиницею питомої теплоти плавлення в системі СІ є джоуль на кілограм (Дж / кг).
згоряння палива
Кількість теплоти, що виділяється при повному згорянні палива масою m,
\ (~ Q = q \ cdot m, \)
де q - питома теплота згоряння (таблична величина).
Одиницею питомої теплоти згорання в СІ є джоуль на кілограм (Дж / кг).
література
Аксеновіч Л. А. Фізика в середній школі: Теорія. Завдання. Тести: Учеб. посібник для установ, що забезпечують отримання заг. середовищ, освіти / Л. А. Аксеновіч, Н.Н.Ракіна, К. С. Фаріно; Під ред. К. С. Фаріно. - Мн .: Адукация i вихаванне, 2004. - C. 129-133, 152-161.









